目前,组织活检是评估肿瘤分子特征的标准生物材料,但仍存在重复取材困难、肿瘤内异质性高等现实问题。液体活检是对肿瘤在体内流出物(主要是血液)中释放的许多成分的分析,来源于肿瘤的循环肿瘤DNA(ctDNA)已被认为是肿瘤生物标志物,可对肿瘤的演变进行动态监测。然而,来源于肿瘤的DNA被体内其他细胞释放的DNA所稀释,ctDNA仅占总游离DNA的0.01%,检测ctDNA需要灵敏度较高的技术,而高灵敏度的dPCR技术在检测ctDNA上具有很大的优势。

应用:ctDNA检测与肿瘤靶向治疗
肺癌是全球死亡率**的恶性肿瘤之一,其中非小细胞肺癌(NSCLC)占肺癌类型的85%。表皮生长因子受体(EGFR)是肺癌的主要驱动基因。EGFR基因突变主要发生在18~21号外显子上,采用EGFR酪氨酸激酶抑制剂(EGFR-TKI)靶向药物治疗会取得比较好的疗效。然而,NSCLC患者在经过靶向治疗后会发生继发性耐药,其中50%~60%为EGFR基因T790M突变,而三代EGFR-TKI 药物AZD9291对这类患者有较好的疗效。因此,进行EGFR基因突变检测对于患者治疗方案的选择以及调整是非常有必要的。
目前,《NSCLC血液EGFR基因突变检测中国专家共识》中推荐可用血浆ctDNA代替肿瘤组织进行EGFR突变检测。利用具有高灵敏度、**定量优势的dPCR技术来检测ctDNA可实现肿瘤的“液体活检”,可达到NSCLC患者的个体化精准治疗。
文献案例1:通过dPCR动态监测血液cfDNA中 EGFR T790M水平,有助于晚期NSCLC患者的EGFR-TKI预后
135例晚期NSCLC患者,同时采用突变扩增系统(ARMS)和dPCR方法对这些患者EGFR-TKI治疗前后血浆中的循环游离DNA(cfDNA)进行T790M突变检测。
结果表明,T790M在不同DNA稀释中的阳性信号比(红/蓝信号)为:1∶100 (115/659)、1∶300 (20/686)、1∶1000 (15/692)、1∶3000 (5/702) (图 1) 和 1∶10000 (0/686)。因此,dPCR检测T790M突变的检出限约为 0.03‰ ,其检出率高于ARMS,更加适用于T790M突变的检测。

通过ARMS和dPCR分别在TKI前和TKI后血浆中检测到T790M 突变(表 2)。在TKI前血浆样本中,ARMS仅在5.5%的患者中检测到T790M (6/103),而dPCR在31.1% 的患者中检测到T790M(32/103)。在135例TKI后血浆样本中,dPCR鉴定出T790M阳性样本的频率高于ARMS(43.0% vs. 25.2%)。

TKI治疗前后血浆cfDNA中T790M突变的频率分别为31%和43%,与在肿瘤组织样本中观察到的频率相似。作为一种高灵敏度和定量的方法,dPCR已被用于评估EGFR突变,血浆cfDNA中的T790M定性和定量可以预测 EGFR-TKI的存活率。此外,动态监测 T790M 变化可能有助于确定 EGFR-TKI 预后。
文献案例2:通过尿液ctDNA检测动态追踪EGFR-TKI治疗NSCLC患者的EGFR突变
选取150例EGFR突变并接受EGFR-TKI的患者参与研究。利用 ddPCR技术量化了尿液、血液中的EGFR突变,并与原发性癌症组织样本做对比。
结果表明,尿液ctDNA在检测EGRF突变方面与组织相比有88%的一致性,且检测灵敏度与血浆结果相当(如图2)。
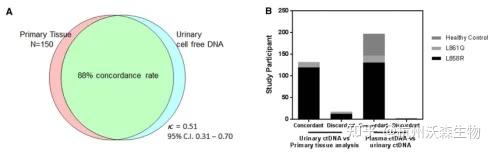
对不同时间点尿液细胞游离 DNA 的分析显示与治疗效果有很强的相关性。在监测过程中,53%的患者检测到继发性EGFR T790M突变,结果与血浆ctDNA分析相印证。T790M阳性突变与野生型组相比,中位生存期降低(图3)。

尿液样本是无创且容易获得的,尿液ctDNA可能是组织样本EGFR突变检测的潜在替代物,利用ddPCR技术来检测尿液ctDNA的EGFR突变可以作为无创监测TKI治疗的有效手段。
参考文献:
[1] Wang Z, Chen R, Wang S, Zhong J, Wu M, Zhao J, Duan J, Zhuo M, An T, Wang Y, Bai H, Wang J. Quantification and dynamic monitoring of EGFR T790M in plasma cell-free DNA by digital PCR for prognosis of EGFR-TKI treatment in advanced NSCLC. PLoS One. 2014 Nov 18;9(11):e110780. doi: 10.1371/journal.pone.0110780. PMID: 25405807; PMCID: PMC4236040.
[2] Chen S, Zhao J, Cui L, Liu Y. Urinary circulating DNA detection for dynamic tracking of EGFR mutations for NSCLC patients treated with EGFR-TKIs. Clin Transl Oncol. 2017 Mar;19(3):332-340. doi: 10.1007/s12094-016-1534-9. Epub 2016 Jul 28. PMID: 27468867.

